Waterstofatoom
Het electron en het proton in een waterstofatoom ondervinden de aantrekking van de coulombkracht. Net als bij een quantumdeeltje in een put zijn de energietoestanden van het waterstof-elektron gequantiseerd:1 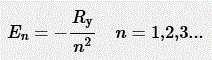
met Ry = 13,61eVde rydberg-energie. Hoe groter n des te dichter liggen de energieniveaus bij elkaar.
In de quantummechanica wordt het waterstof-electron beschreven met een golffunctie ψ.
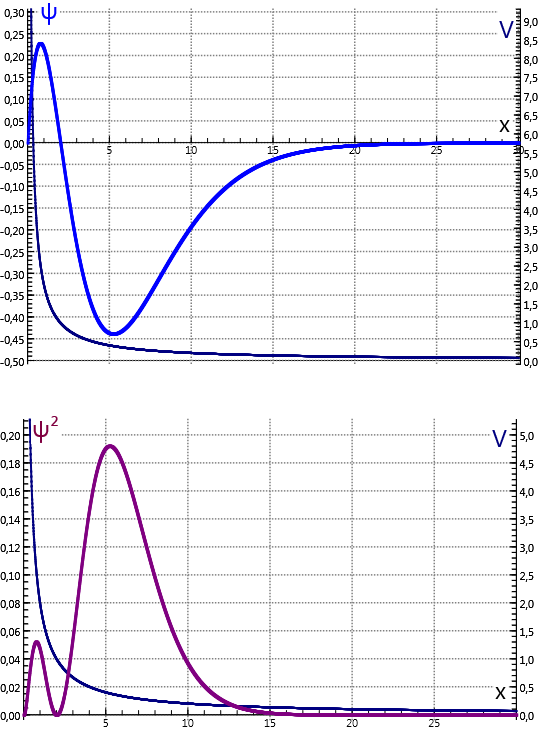
De kans om het elektron op een afstand r van de kern aan te treffen wordt gegeven door het kwadraat van de golffunctie |ψ(r)|2.
In de grondtoestand ligt het maximum bij de 'bohrstraal' a0 ≃ 5,29 ⋅ 10−2nm, zoals in het voorbeeld berekend wordt.2Ter vereenvoudiging van de modelregels worden dimensieloze variabelen geintroduceerd.
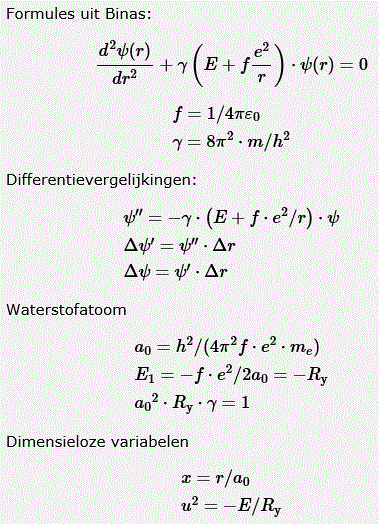
Modelregels
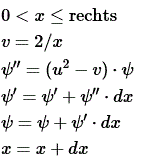
Download coachbestand met tekstuele model (cma7, 523 kB)
Grafisch model
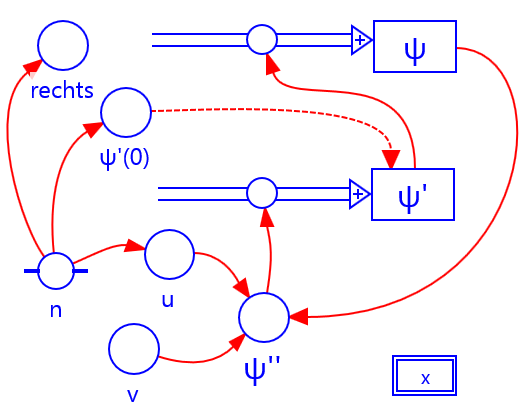
Download coachbestand met grafisch model (cma7, 534 kB)
Voorbeeld
Startwaarden
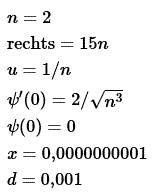
1. H. van Bemmel en L. Koopman, Nova natuurkunde 6 vwo, Malmberg (2015)
2. Waterstofatoom (pdf, 1.5 MB), Voorbeeldexamenopgaven quantumwereld natuurkunde vwo (2016)